埃索美拉唑
| 中文名称 | 埃索美拉唑 |
|---|---|
| 中文同义词 | 埃索美拉唑锶;艾司奥美拉唑钠;埃索美拉唑EP杂质F;埃索美拉唑;艾司奥美拉唑;5-甲氧基-2-((S)-((4-甲氧基-3,5-二甲基-2- 吡啶基)甲基)亚硫酰基)-1H-苯并咪唑;埃索美拉唑微丸8.5%;埃索米拉唑 |
| 英文名称 | Esomeprazole |
| 英文同义词 | EsoMeprazole EC Pellets 22%;EsoMaprozole;1H-BenziMidazole,6-Methoxy-2-[(S)-[(4-Methoxy-3,5-diMethyl-2-pyridinyl)Methyl]sulfinyl]-;EsoMeprazole EC Pellets 8.5%;6-Methoxy-2-{(S)-[(4-Methoxy-3,5-diMethyl-2-pyridinyl)Methyl]sulfinyl}-1H-benziMidazole;Esomeprazole(Na、Mg);(5-methoxy-1H-benzimidazol-2-yl)[(4-methoxy-3,5-dimethylpyridin-2-yl)methyl]sulfoniumolate;(S)-Esomeprazole |
| CAS号 | 119141-88-7 |
| 分子式 | C17H19N3O3S |
| 分子量 | 345.42 |
| EINECS号 | 643-098-6 |
| 相关类别 | 医药原料药;医药杂质;杂质;医药中间体;杂质对照品;原料药;医药原药;医药原料;医用原料;化工原料;医药原料;化工中间体;API;原料中间体-原料药 |
| Mol文件 | 119141-88-7.mol |
| 结构式 | 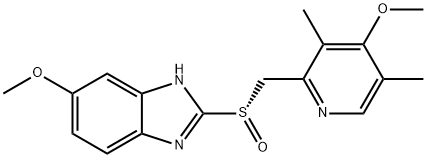 |
埃索美拉唑 性质
| 比旋光度 | D20 -155° (c = 0.5 in chloroform) |
|---|---|
| 沸点 | 600.0±60.0 °C(Predicted) |
| 密度 | 1.37±0.1 g/cm3(Predicted) |
| 储存条件 | Sealed in dry,Room Temperature |
| 溶解度 | DMF: 30 mg/ml,DMSO: 20 mg/ml,乙醇: 10 mg/ml,PBS (pH 7.2): 10 mg/ml |
| 形态 | 固体 |
| 酸度系数(pKa) | 8.50±0.10(Predicted) |
| CAS 数据库 | 119141-88-7(CAS DataBase Reference) |
埃索美拉唑(英文Inexium)又称为艾美拉唑、艾司奥美拉唑、埃索他拉唑、艾司奥美拉唑镁、左旋奥美拉唑,是奥美拉唑的S-异构体,1990年,体外胃腺模型证实奥美拉唑的两种异构体具有相同的质子泵抑制作用。然而,当时不可能制备足够数量的单一异构体用于体内试验,分离的异构体在水溶液中可缓慢消旋化。当有足够数量的两种异构体用于人体研究时,显示口服S-异构体的作用约比R-异构体高4倍。埃索美拉唑通过特异性的靶向作用机制减少胃酸分泌,为壁细胞中质子泵的特异性抑制剂,呈弱碱性,在壁细胞泌酸微管的高酸环境中浓集并转化为活性形式,从而抑制该部位的H/K-ATP酶(质子泵),对基础胃酸分泌和刺激的胃酸分泌均产生抑制。对胃食管反流病治疗在症状缓解、抑制胃酸、促进食管炎改善方面均优于奥美拉唑。
【类 别】 抗溃疡药,质子泵抑制剂
【CAS】 119141-88-7
【研制单位】 瑞典Astra Zeneca公司
【上市国家及年份】 瑞典,2000年
【性 状】 无色浆状物,[α]D20-155°(c= 0.5,氯仿)
【专 利】 EP5129埃索美拉唑(Esomeprazole)即(S)?奥美拉唑,分子量为345.41600,密度为1.37g/cm3,沸点为600ºC at 760mmHg,闪点为316.7ºC,折射率为1.669,蒸汽压为0mmHg at 25°C,为白色或类白色的冻干块状物或粉末。其可有效地抑制胃酸分泌,常用于治疗与胃酸分泌紊乱有关的疾病。给SD大鼠静脉注射14C标记的埃索美拉唑5mg/kg后,雌鼠的血浆药物半衰期为7.3h,雄性大鼠为17.4h。经口给药吸收迅速,血浓峰值呈双峰,分别出现在药后1h和4h。经大鼠胆管引流实验发现,用药后的吸收过程持续时间达24h以上。药物在全身各器官组织的浓度高低顺序为:肝>肾>肺>血液>脂肪。经口给药后药物的排泄以粪便排泄为主。埃索美拉唑的药动学曲线呈线性,当给药量增加时,其AUCs和cmax也相应增加,而tmax,CL和半衰期则无明显改变。
该药毒性较低,大鼠经口给药的LD50大于5g/kg,腹腔给药的LD50亦在2.5g/kg以上。实验犬以10mg/kg的剂量连续服用28d,未见明显异常。大鼠连续用药13周,在剂量为80mg/kg时,所有生理参数均无改变,致毒剂量在320mg/kg以上。在一般药理实验中,本品对心血管及植物神经系统影响极小,仅在高剂量下对中枢神经系统有轻微影响。埃索美拉唑是奥美拉唑的S型光学异构体,其特点是口服后首过效应少,生物利用度和血浓度较奥美拉唑或R型异构体高,特异性抑制胃壁细胞中质子泵,抑酸药效强而持久。本品在小肠吸收。单次口服1~2小时内血药浓度达峰值,生物利用度为64%,连续用药则提高到90%。进食后服药降低生物利用度。本品在肝内经细胞色素P450酶系完全代谢,80%由尿排出,余经粪排泄;仅1%以原形经肾排泄。本品口服吸收的个体差异小,故对疗效的预测性好。
药效学特性埃索美拉唑是奥美拉唑的S-异构体,通过特异性的靶向作用机制减少胃酸分泌,为壁细胞中质子泵的特异性抑制剂。奥美拉唑的R-异构体和S-异构体具有相似的药效学特性。1.胃食管反流性疾病 (GERD)【类 别】 抗溃疡药,质子泵抑制剂
【CAS】 119141-88-7
【研制单位】 瑞典Astra Zeneca公司
【上市国家及年份】 瑞典,2000年
【性 状】 无色浆状物,[α]D20-155°(c= 0.5,氯仿)
【专 利】 EP5129埃索美拉唑(Esomeprazole)即(S)?奥美拉唑,分子量为345.41600,密度为1.37g/cm3,沸点为600ºC at 760mmHg,闪点为316.7ºC,折射率为1.669,蒸汽压为0mmHg at 25°C,为白色或类白色的冻干块状物或粉末。其可有效地抑制胃酸分泌,常用于治疗与胃酸分泌紊乱有关的疾病。给SD大鼠静脉注射14C标记的埃索美拉唑5mg/kg后,雌鼠的血浆药物半衰期为7.3h,雄性大鼠为17.4h。经口给药吸收迅速,血浓峰值呈双峰,分别出现在药后1h和4h。经大鼠胆管引流实验发现,用药后的吸收过程持续时间达24h以上。药物在全身各器官组织的浓度高低顺序为:肝>肾>肺>血液>脂肪。经口给药后药物的排泄以粪便排泄为主。埃索美拉唑的药动学曲线呈线性,当给药量增加时,其AUCs和cmax也相应增加,而tmax,CL和半衰期则无明显改变。
该药毒性较低,大鼠经口给药的LD50大于5g/kg,腹腔给药的LD50亦在2.5g/kg以上。实验犬以10mg/kg的剂量连续服用28d,未见明显异常。大鼠连续用药13周,在剂量为80mg/kg时,所有生理参数均无改变,致毒剂量在320mg/kg以上。在一般药理实验中,本品对心血管及植物神经系统影响极小,仅在高剂量下对中枢神经系统有轻微影响。埃索美拉唑是奥美拉唑的S型光学异构体,其特点是口服后首过效应少,生物利用度和血浓度较奥美拉唑或R型异构体高,特异性抑制胃壁细胞中质子泵,抑酸药效强而持久。本品在小肠吸收。单次口服1~2小时内血药浓度达峰值,生物利用度为64%,连续用药则提高到90%。进食后服药降低生物利用度。本品在肝内经细胞色素P450酶系完全代谢,80%由尿排出,余经粪排泄;仅1%以原形经肾排泄。本品口服吸收的个体差异小,故对疗效的预测性好。
胃食管反流病(GERD)是由于胃内容物反流入食管引起胃灼热、反酸、胸骨后疼痛等症状,并造成食管黏膜病理性损害,是临床常见酸相关性疾病之一,抑制胃酸是胃食管反流病治疗的关键。埃索美拉唑(eaomeprazole)是奥美拉唑(耐信)的左旋异构体,起效快、抑酸效果好,用于治疗反流性食管炎,单用或联合消化道促动力药或消化道粘膜保护剂,疗效均优于其他PPI(埃索美拉唑、兰索拉唑、奥美拉唑、泮托拉唑、雷贝拉唑),对老年反流性食管炎及儿童反流性食管炎安全有效。
2.糜烂性反流性食管炎的治疗
3.已经治愈的食管炎患者防止复发的长期维持治疗
4.胃食管反流性疾病 (GERD) 的症状控制与适当的抗菌疗法联合用药根除幽门螺杆菌
5.愈合与幽门螺杆菌感染相关的十二指肠溃疡
6.防止与幽门螺杆菌相关的消化性溃疡复发药片应和液体一起整片吞服,而不应当咀嚼或压碎。
胃食管反流性疾病 (GERD)
1.糜烂性反流性食管炎的治疗,40mg 每日一次,连服四周。
2.对于食管炎未治愈或持续有症状的患者建议再服药治疗四周。已经治愈的食管炎患者防止复发的长期维持治疗,20mg每日一次。
3.胃食管反流性疾病 (GERD) 的症状控制
没有食管炎的患者 20mg 每日一次。如果用药4周症状未获控制,应对患者作进一步的检查。一旦症状消除,随后的症状控制可采用即时疗法,即需要时口服 20mg ,每日一次。
4.与适当的抗菌疗法联合用药根除幽门螺杆菌,并且愈合与幽门螺杆菌相关的十二指肠溃疡,预防与幽门螺杆菌相关的消化性溃疡复发,埃索美拉唑片 20 mg + 阿莫西林 1 g + 克拉霉素 500mg ,每日二次,共7天。本品可降低酮康唑和伊曲康唑的吸收。与本品合用时,应减少经CYP2C19酶代谢的药物,如地西洋,西酞普兰,丙米嗪,氯米帕明和苯妥英的剂量。当与本品合用或停用本品时,应监测苯妥英的血浆浓度。
本品与阿莫西林、奎尼丁或华法林之间无相互作用,且与克拉霉素同用无需调整剂量。
服用本品过量的临床资料不多,但是本品单一剂量80mg未见不良反应。本品没有特殊的解毒剂。这些反应均没有剂量相关性。
常见反应(>1/100,<1/10):头痛、腹痛、腹泻、腹胀、恶心/呕吐、便秘。
少见反应(>1/1000,<1/100):皮炎、瘙痒、荨麻疹、头昏、口干。
在消旋体(奥美拉唑)的使用中曾观察到下列不良反应,因而在埃索美拉唑的使用中也可能发生。
生产方法
从奥美拉唑拆分得到。
安全信息
| 海关编码 | 29339900 |
|---|---|
| 毒害物质数据 | 119141-88-7(Hazardous Substances Data) |
